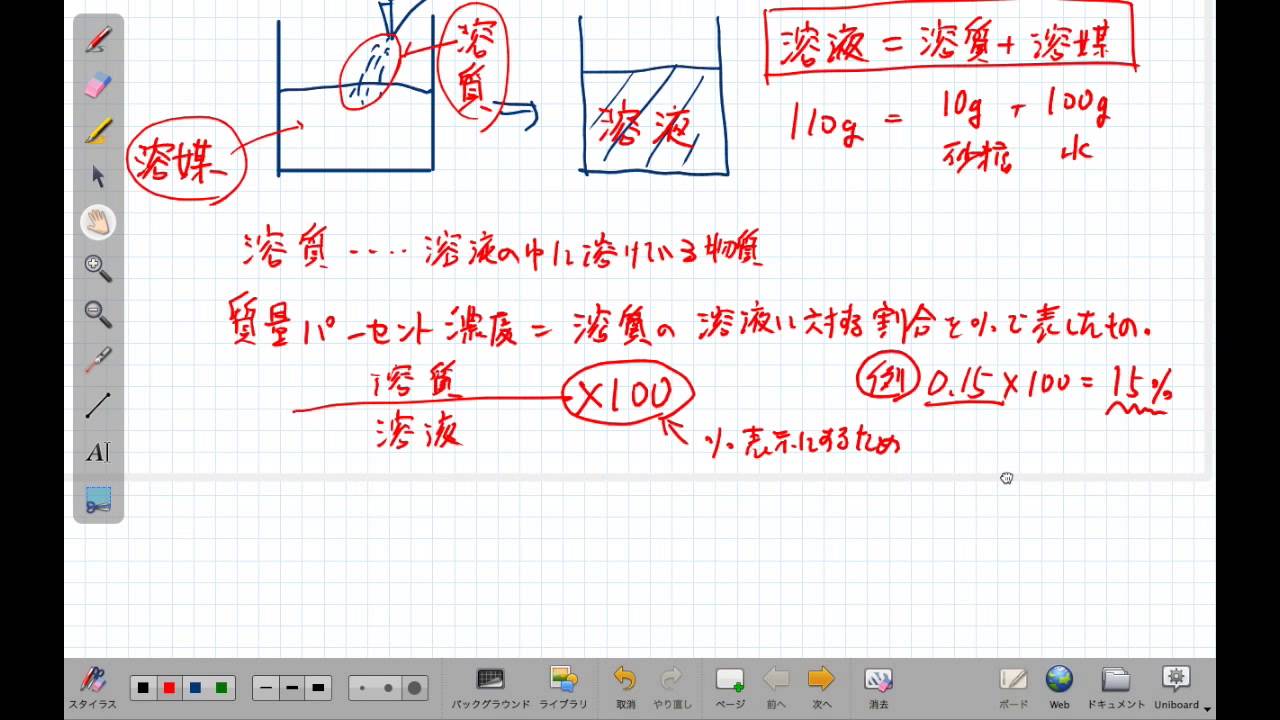
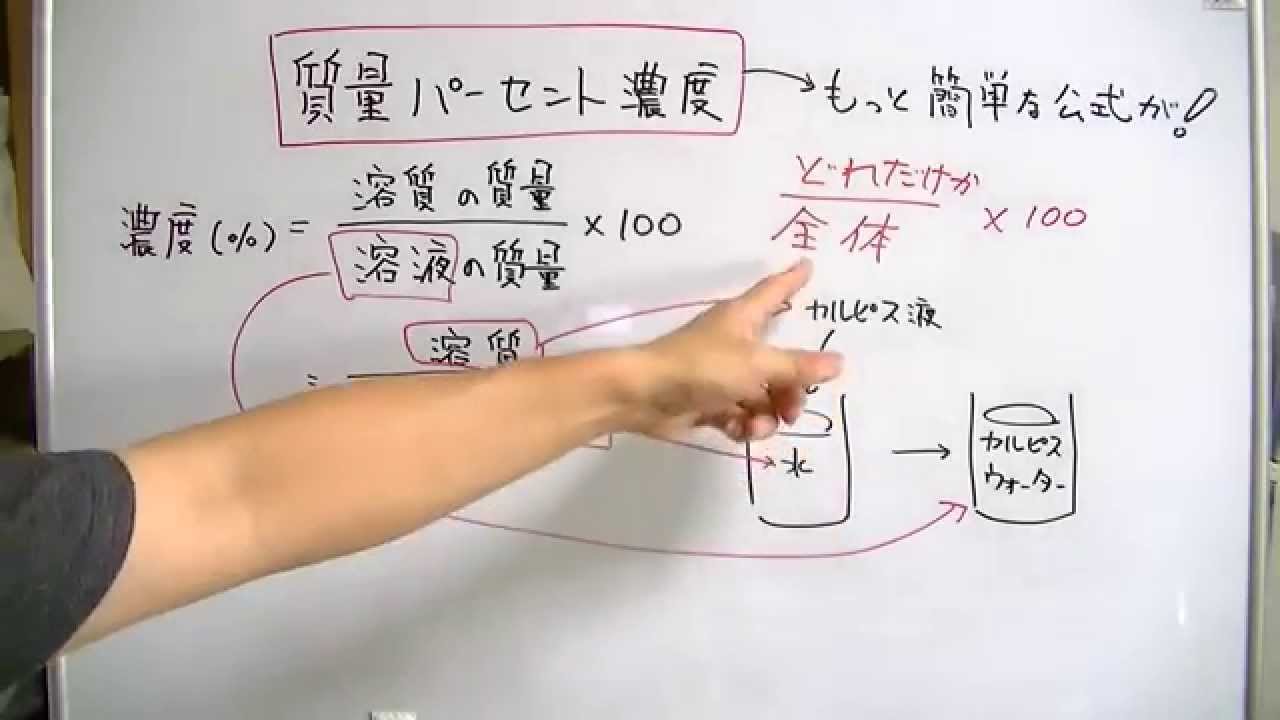
「日本薬局方で定める濃度の範囲 ≒ およそ②質量百分率で70%くらい」ということから、一般的に「70%のエタノール」という言い方をよくされるのだと思われます。 「70%以下」の濃度では意味がない?質量パーセント濃度 質量パーセント濃度 とは、その名の通り質量を使って求めた濃度です。 単位は%を使います。 溶液の質量に対して溶質が何g溶けているかを百分率で表したもの です。 次の計算式で求めることができます。溶質の質量を求める 水溶液の濃度の応用問題では、いつも真っ先に 「溶質は何gとけているだろう?」 「水溶液全体の質量は何gだろう?」 の2つを考えることができれば大丈夫です。

中1理科 水溶液の性質 問題集 中学生 理科のノート Clear
質量 パーセント 濃度 の 求め 方
質量 パーセント 濃度 の 求め 方-質量パーセント濃度 質量パーセント濃度 とは、その名の通り質量を使って求めた濃度です。 単位は%を使います。 溶液の質量に対して溶質が何g溶けているかを百分率で表したもの です。 次の計算式で求めることができます。はじめに ここでは、溶液の濃度を表す単位である質量パーセント濃度、モル濃度そして質量モル濃度の単位、求め方についてまとめています。 質量パーセント濃度 小学校や中学校で、食塩水の濃度を求めてみましょうという問題を解いたのを記憶しれいる人も多いかと



4番教えてください 計算の仕方がわからないです Clear
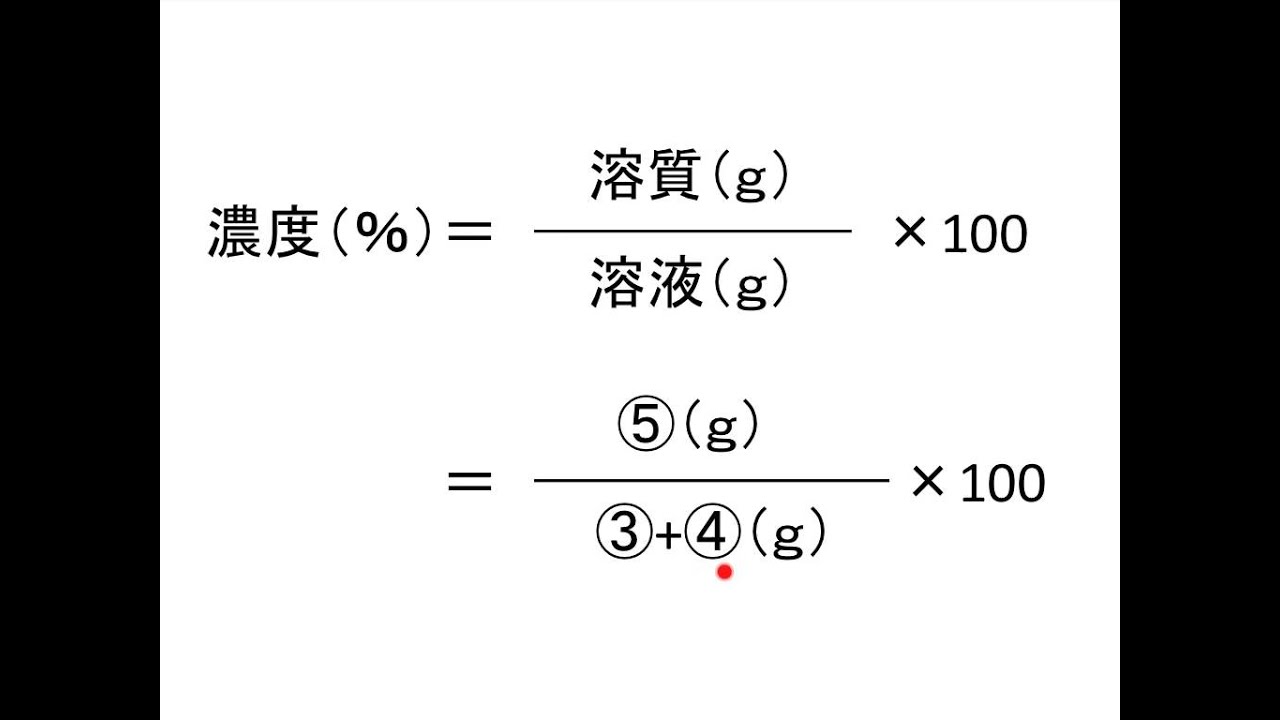
Vol% ⇒ 体積で計算した濃度の単位 wt% ⇒ 質量(重量)で計算した濃度の単位 % ⇒ 全体を100にして考えた時の割合 ppm ⇒ 濃度を表す単位で100万分の1のこと。1 vol%=ppm %(百分率)、wt%の意味など下記も参考になります。 百分率とは?最初に触れましたが、質量パーセント濃度は以下の式で求められます。 質量パーセント濃度(%)= 溶質の質量(g)÷ 溶液(溶質溶媒)の質量(g)×100 これは、溶液の中に溶けている溶質が全体の何パーセントかということです。JIS K 0211 13 「分析化学用語(基礎部門)」 質量分率,質量パーセント濃度( mass fraction ) 質量単位を用いて表したある成分の全体に対する比率。質量分率 0123,質量分率 123 %などと表す。
質量パーセント濃度の求め方 質量パーセント濃度とは、 その液体がどれくらい濃いか? を表した数値です。 数値が高い方が、たくさんのモノが溶けており濃い!ということを表しています。質量/体積(容積)パーセント濃度の求め方 溶質の質量(g) ÷ 溶液の体積・容積(ml) × 100 = 質量/体積パーセント濃度 % 体積(容積)ml にしめる、溶質の割合を求める方法です。さてまずは質量パーセント濃度から。 これは中学1年生のみなさんがちょうど習っている内容かもしれませんね。 さて、質量パーセント濃度とはいったい何なのでしょうか? 質量パーセント濃度とは「 ある溶液中に溶けている溶質の割合 」を示します。
溶液の濃度とその表し方 1原子量と分子量 定義・説明 原子量は質量数12の炭素同位体( )の質量を12とした時の、他の元素の相対的質量である。 したがって、原子量は無次元で単位はない。一般に,溶液中に含まれる溶質の割合を濃度といい,その表し方には,質量パーセント濃度,モル濃度, 質量モル濃度などがある。濃度に関する出題タイプは,主にⅠ~Ⅶの7つのタイプがある。 例えば,食塩(NaCl)を水(H 2O)に溶かした食塩水を考える。質量パーセント濃度98%、密度184g/cm 3 の濃硫酸(分子量98)のモル濃度を求めよ。 とりあえず密度と分子量を使って計算式を立てる。 基本これを計算すれば終了なんだけど、今回は 質量パーセント濃度の記載があるのでそれを掛けてあげる。
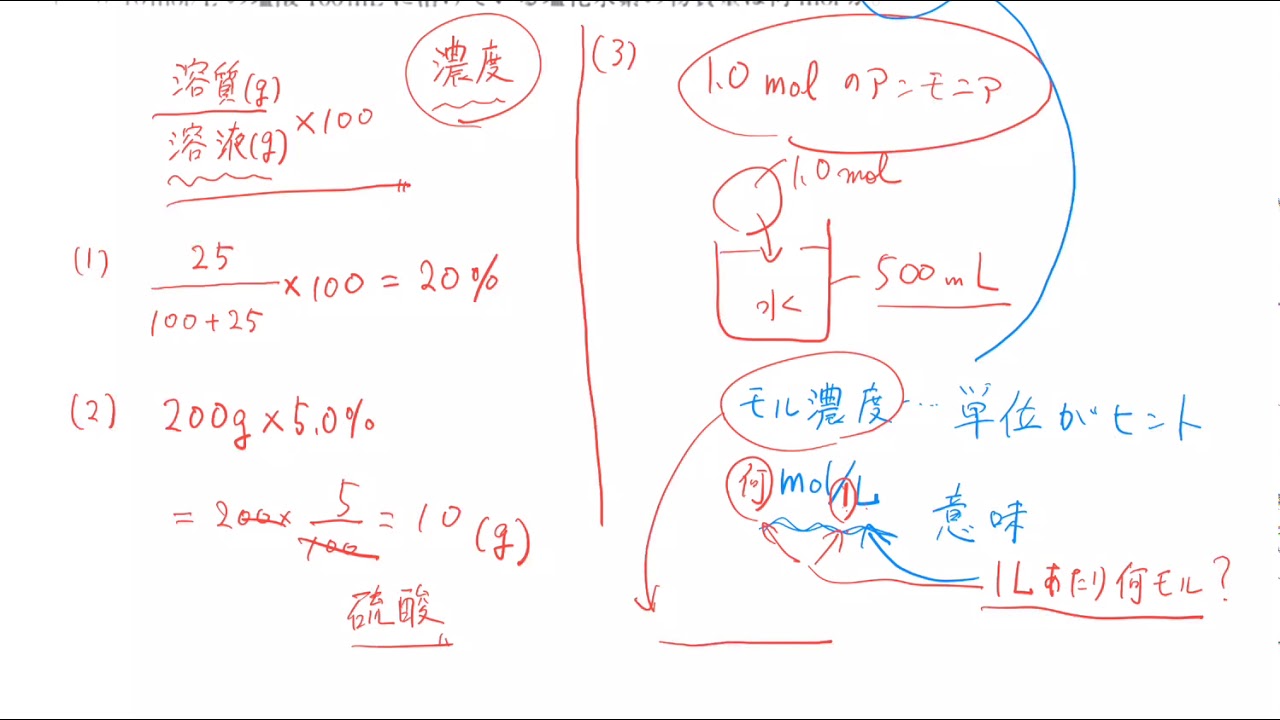


質量パーセント濃度とモル濃度の問題 Youtube



中1理科 水溶液の性質 問題集 中学生 理科のノート Clear
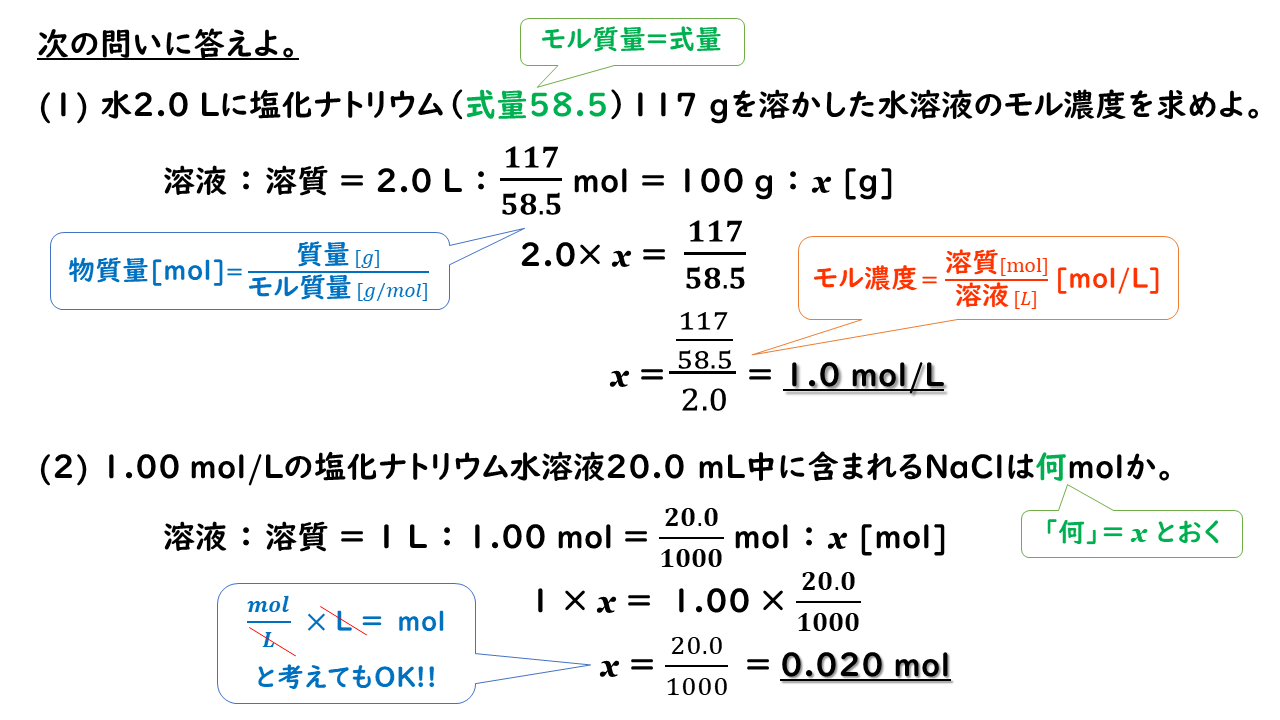
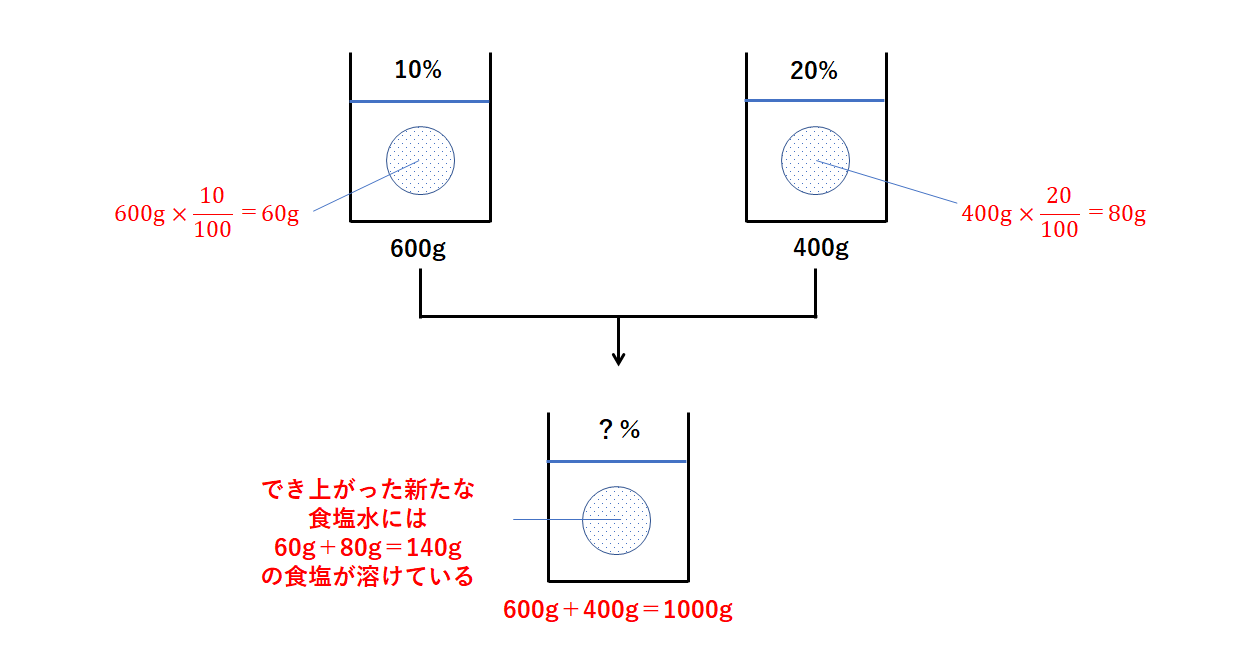
この砂糖水の質量パーセント濃度は何%か。 (3) 100gの水に60gの砂糖を入れてつくった砂糖水の質量パーセント濃度は何%か。 次の問いに答えよ。 (1) 質量パーセント濃度4%の塩化ナトリウム水溶液を250g作る場合 塩化ナトリウムは少なくとも何g必要か。溶質の質量を求める 水溶液の濃度の応用問題では、いつも真っ先に 「溶質は何gとけているだろう?」 「水溶液全体の質量は何gだろう?」 の2つを考えることができれば大丈夫です。溶液は、(溶媒溶質 )のことです~ 0 麻美 4年以上前 分かりました!それでは溶媒や溶質の求め方を教えてください。



Hd限定理科 質量 パーセント 濃度 問題 ただぬりえ



理科 中1 27 質量パーセント濃度 Youtube
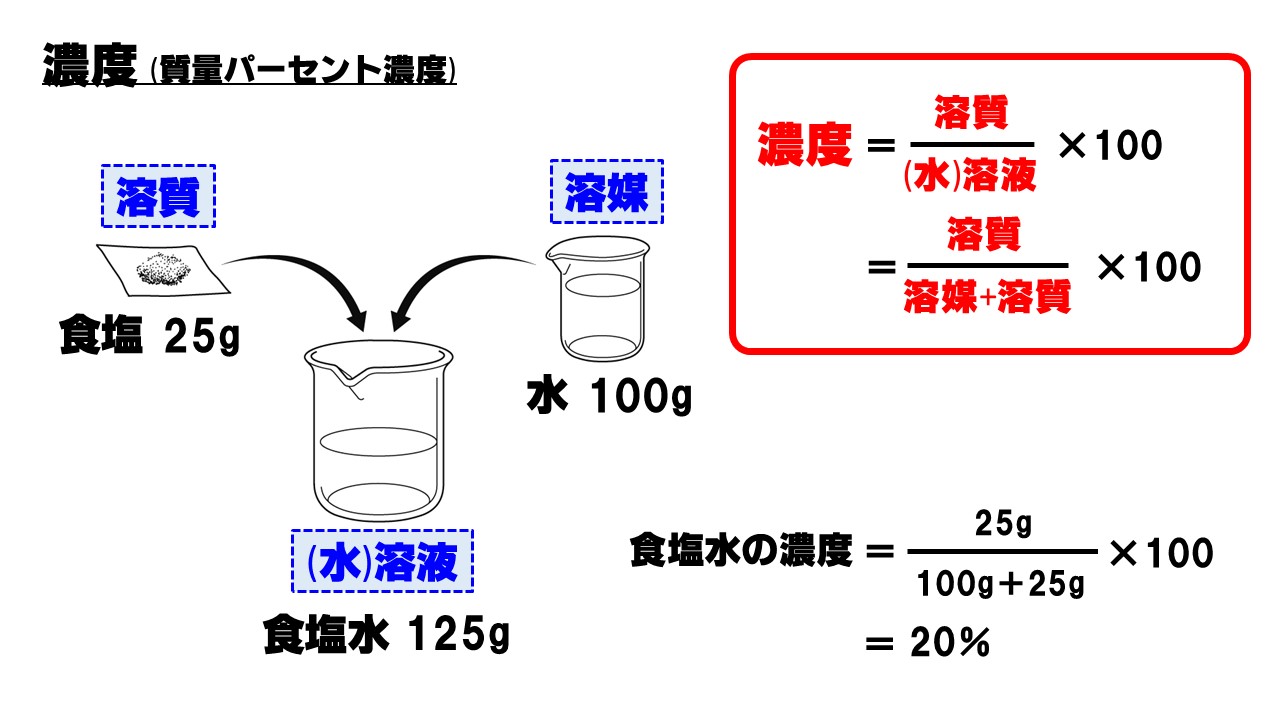
質量パーセント濃度とは 次は"質量パーセント濃度"にうつりましょう。 単位:g/g→% $$\frac{溶質の質量(g)}{溶液の質量(g)}\times 100=\%$$ これも非常に単純で、溶液の質量(g)を分母、溶質の質量(g)を分子に持って来た上で「割合」を求めます。反応が100%進めば、S1モル(32g)を使ってh₂so₄1モル(98g)が生成します。 s→so₂→h₂so₃→h₂so₄ そこで 「自分ではまず18×1000=1800g このうち98%が濃硫酸だから、 1800×098=1764g がh2so4 であることまでは求めた」 これは1Lの濃硫酸に含まれているh2so4の質量ですよね。動画一覧や問題のプリントアウトはこちらをご利用ください。ホームページ → http//19chtv/ Twitter→ https//twittercom/haichi_toaru



中1理科 濃度の計算 映像授業のtry It トライイット


受験基礎化学 18 溶液の濃度 みかみの参考書ブログ
さてまずは質量パーセント濃度から。 これは中学1年生のみなさんがちょうど習っている内容かもしれませんね。 さて、質量パーセント濃度とはいったい何なのでしょうか? 質量パーセント濃度とは「 ある溶液中に溶けている溶質の割合 」を示します。質量パーセント濃度の求め方の計算公式って?? こんにちは!この記事を書いてるKenだよ。ペットボトル、固いね。 質量パーセント濃度の求め方の公式は、 (質量パーセント濃度 % )= (溶質の質量)÷(溶液の質量)×100 だ。



溶液の濃度に関する問題 完全攻略チャート 過去問解説集 自宅でできる受験対策ショップ ワカルー Wakaru
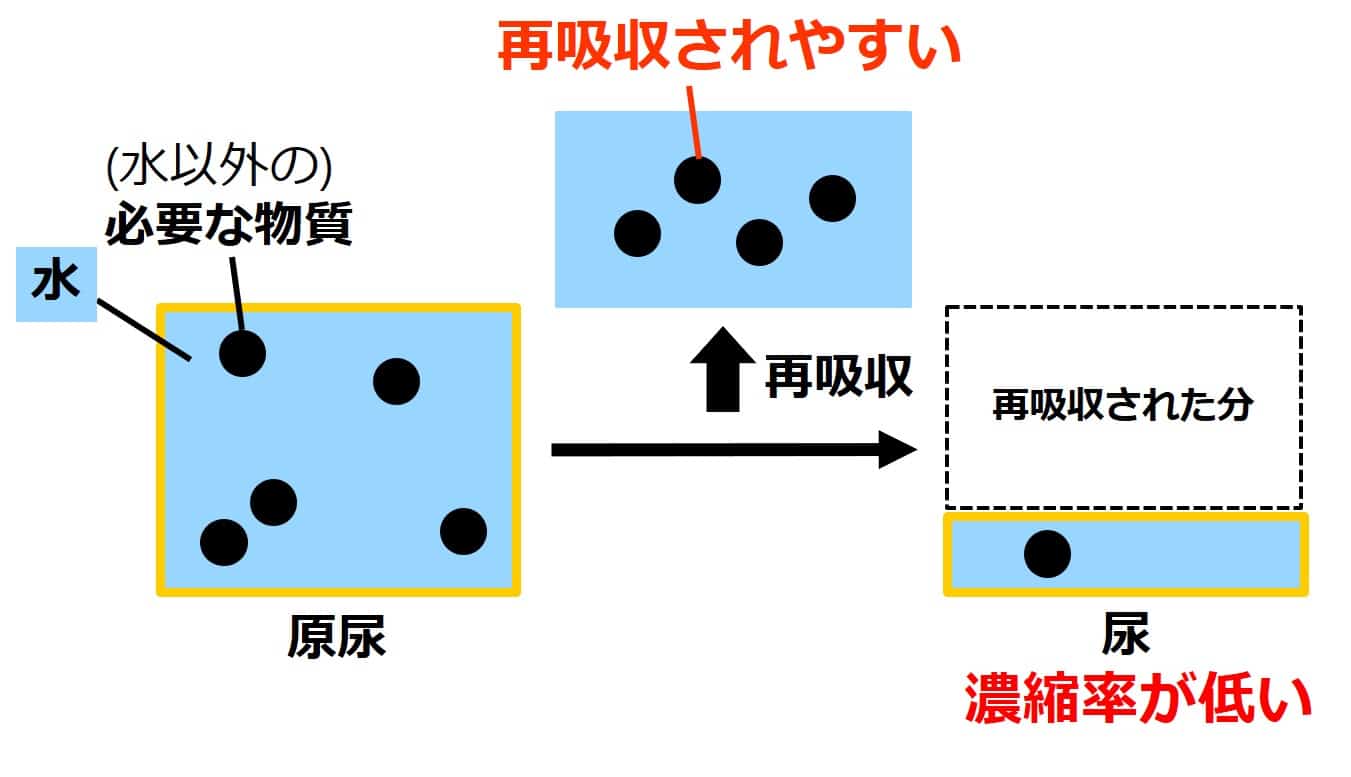


腎臓 計算に必要な基礎知識 濃縮率の求め方 せいぶつ農国



高校化学基礎 質量パーセント濃度とは 映像授業のtry It トライイット
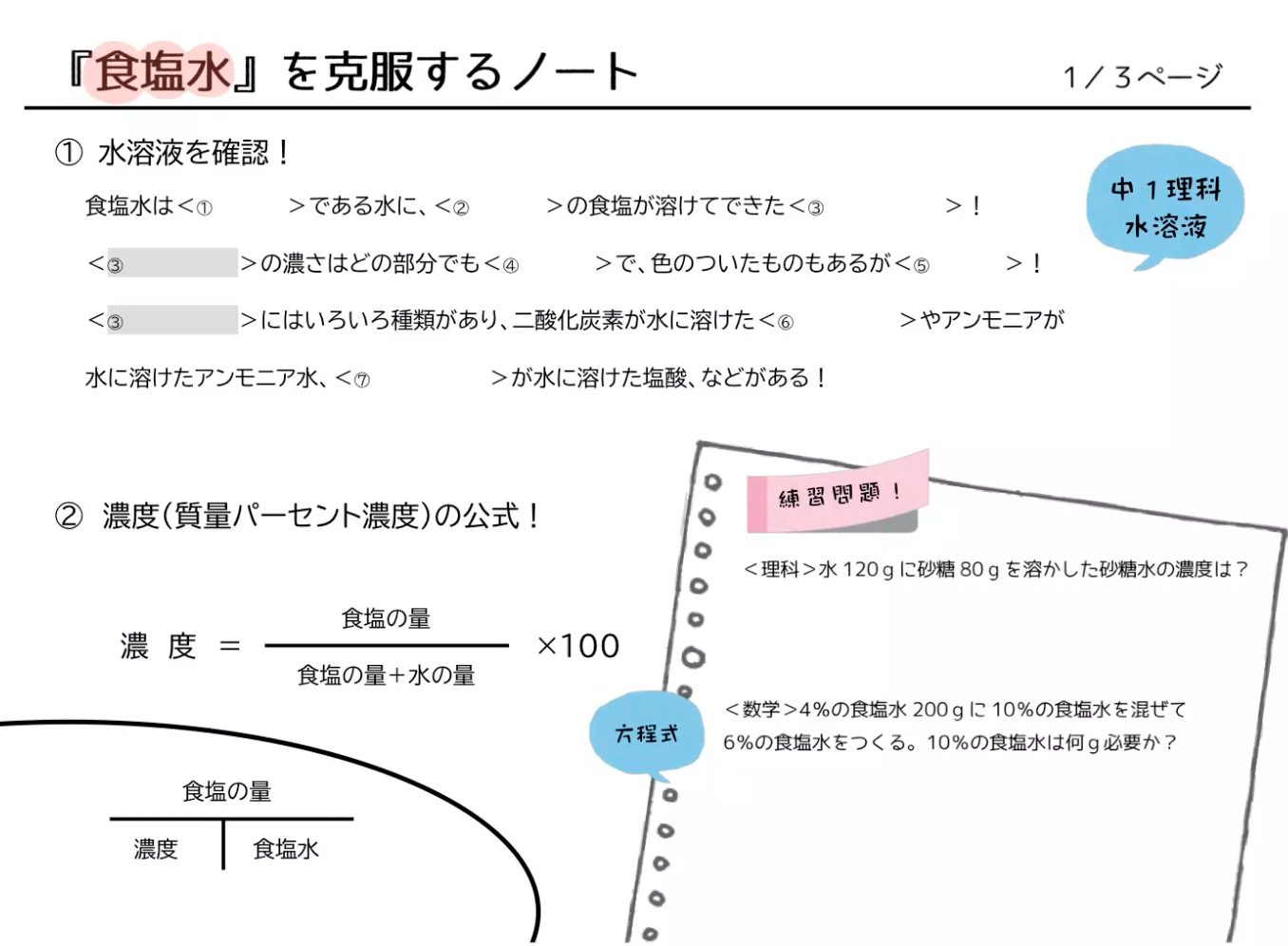


中1理科 数学 食塩水の問題を動画でマスター 公式の覚え方と濃度の計算 マナブレイン



モル濃度とは 計算 求め方 公式はコレで完璧 質量パーセントとの違いも 高校生向け受験応援メディア 受験のミカタ



西村能一 科学の名著50冊が1冊でざっと学べる Kadokawa 化学計算問題 4 濃度 Mol L Mol Kgを 求める 水酸化ナトリウム25gを水100gに溶解させた溶液の密度が1 2 G Cm3であった 1 この水溶液の質量パーセント濃度は何 か 2 この水溶液



理科 中1 質量パーセント濃度 問題 中学生 理科のノート Clear



中1理科 水溶液の濃度の求め方 食塩水 Youtube



質量パーセント濃度に関する質問 2ページ 勉強質問サイト



溶質 溶媒 溶液 塾の質問箱



高校生物基礎 腎臓のイヌリン濃縮率や原尿量などの計算問題の解き方 高校生物の学び舎
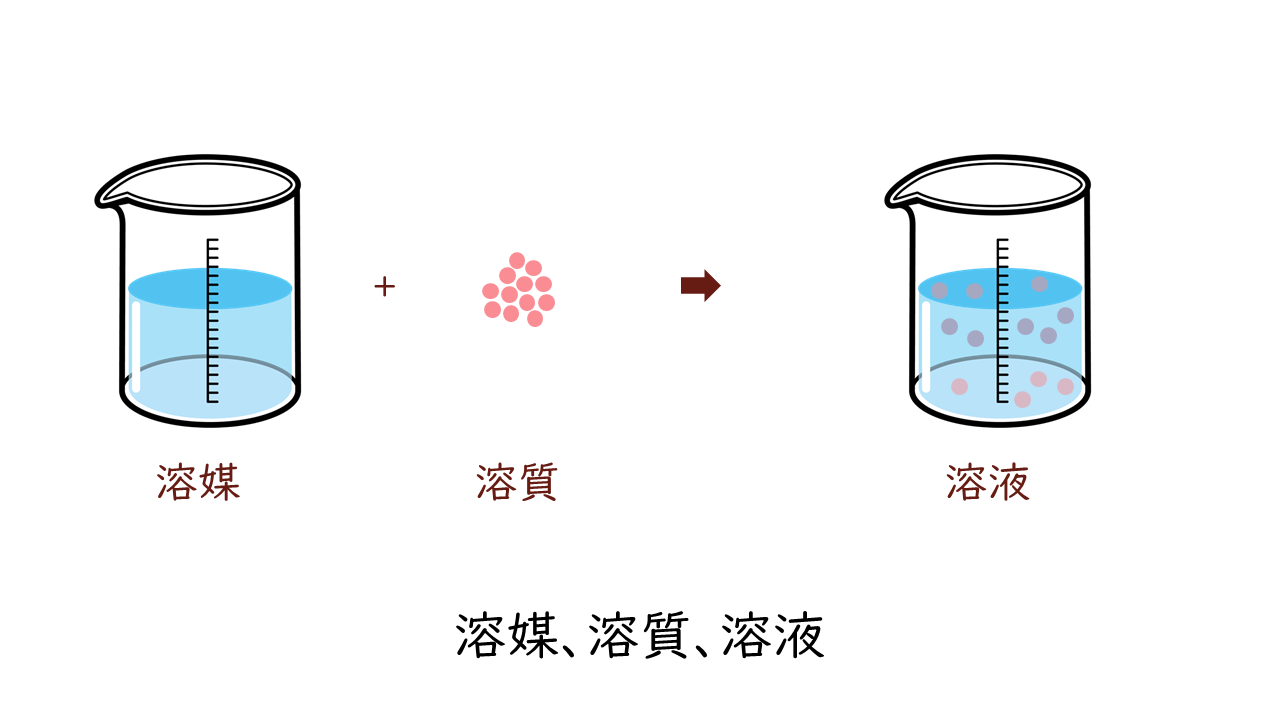


溶液 濃度 気になる遺伝子


4 6 溶液の濃度 おのれー Note


Ph中和 基礎の基礎 Mol濃度とは 流体技術マガジン



濃度 の計算が苦手な方へ 元研究員がわかりやすく解説 Study Z ドラゴン桜と学ぶwebマガジン



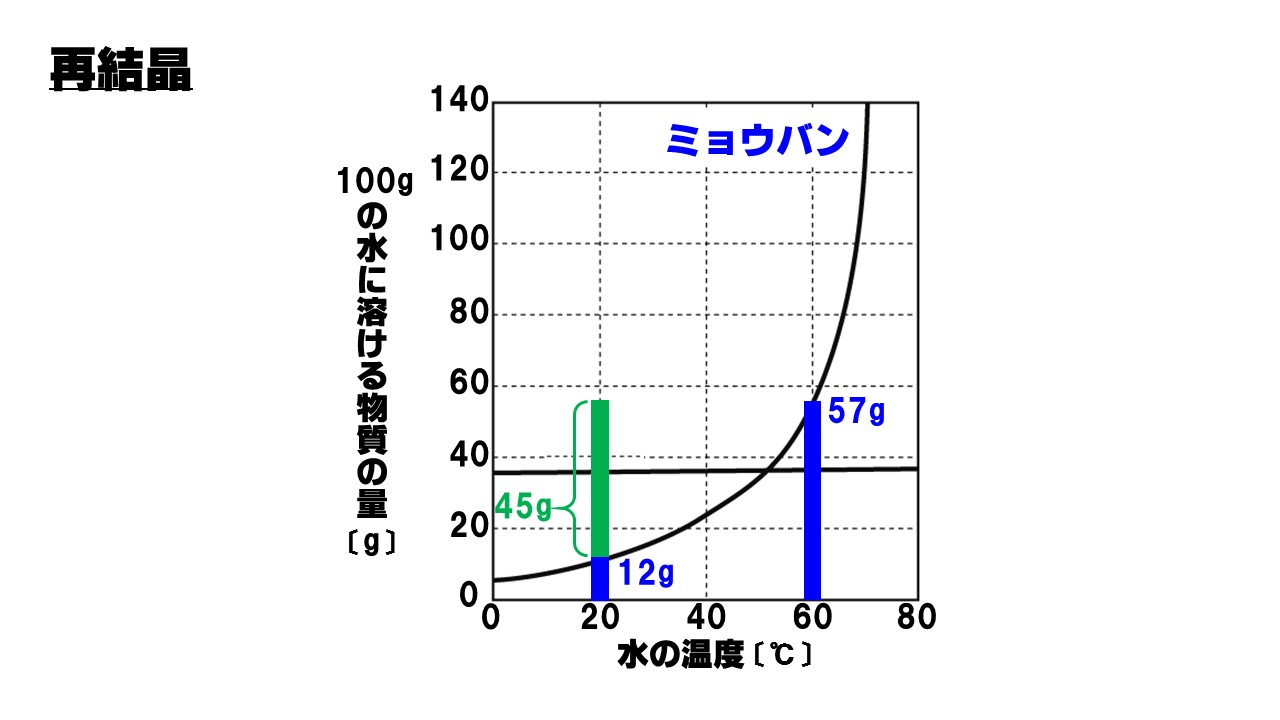
中1理科 溶解度の求め方と練習問題 中学生勉強サイトあかね先生



高校化学基礎 質量パーセント濃度とは 映像授業のtry It トライイット



美しい 水溶液 の 濃度 計算 壁紙 配布



1 60 で水100gに硫酸銅 五水和物cuso 5h Oを30g溶解させた この溶液の質量パーセント濃度は何 か 硫酸銅 五水和物に関する問題 Youtube


中1理科 身の回りの物質 質量パーセント濃度 Youtube



中1理科 質量パーセント濃度の求め方 やすひこ先生の中学生授業log



モル濃度とは 計算 求め方 公式はコレで完璧 質量パーセントとの違いも 高校生向け受験応援メディア 受験のミカタ



7 8 9 2が分かりません 教えて下さい Clear



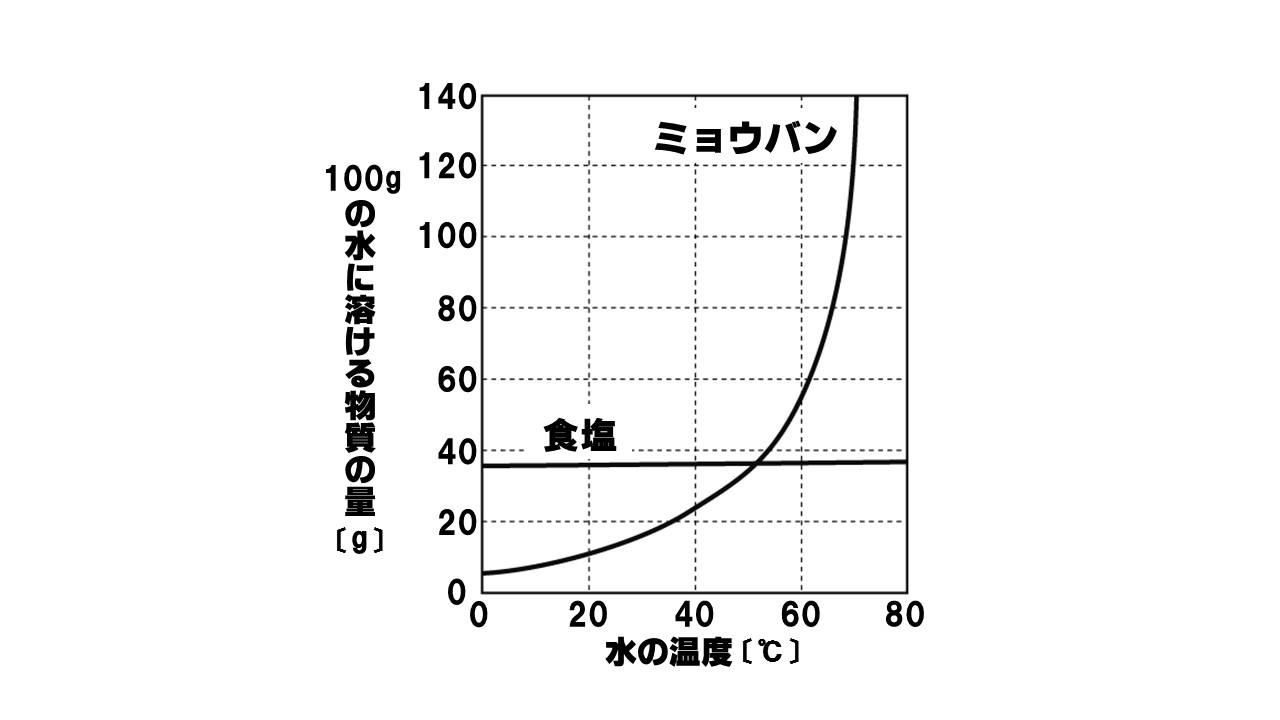
中1理科 テストに出やすい 溶解度曲線の問題の解き方 Qikeru 学びを楽しくわかりやすく



化学基礎の質量パーセント濃度 化学に関する質問 勉強質問サイト



質量パーセント濃度 化学に関する質問 勉強質問サイト



質量パーセント濃度 求め方 計算 高校化学 エンジョイケミストリー Youtube



水溶液の計算 理科に関する質問 勉強質問サイト



4番教えてください 計算の仕方がわからないです Clear



4 6 溶液の濃度 おのれー Note



濃度計算 化学に関する質問 勉強質問サイト



質量パーセント濃度 化学に関する質問 勉強質問サイト



高校理論化学 食酢中の酢酸のモル濃度と質量パーセント濃度 受験の月



ジュピターノート 108 モル濃度計算の仕方とパターンの解説 共通テスト 2次試験対 Clear



高校化学基礎 密度とモル濃度 映像授業のtry It トライイット



高校理論化学 溶液の濃度と調製 質量パーセント濃度 密度とモル濃度の単位換算 受験の月



モル濃度 質量モル濃度 化学に関する質問 勉強質問サイト



質量パーセント濃度のやつだと思います 1 は15gで合ってますか 2 の解き方が分からないです 分かる方お願いします 高校数学に関する質問 勉強質問サイト



化学基礎 モル濃度と質量パーセント濃度の計算問題 Tekibo


最新のhd 物質 の 質量 の 求め 方 壁紙 配布



溶液 濃度 気になる遺伝子



高校化学基礎 硫酸とモル濃度 映像授業のtry It トライイット


濃度の求め方 絵で覚えよう Youtube


壁紙 押入れ 50 溶液 の 質量 の 求め 方



理科 中1 質量パーセント濃度 問題 中学生 理科のノート Clear



中1 理科 質量パーセント濃度の計算 P塾



高校化学基礎 モル濃度の計算 練習編 映像授業のtry It トライイット



5分でわかる モル濃度 溶液1l中に溶質が何モル溶けている 元研究員がわかりやすく解説 Study Z ドラゴン桜と学ぶwebマガジン



モル濃度とは 計算 求め方 公式はコレで完璧 質量パーセントとの違いも 高校生向け受験応援メディア 受験のミカタ


中1化学 水溶液 濃度 中学理科 ポイントまとめと整理



高校化学 質量モル濃度 映像授業のtry It トライイット



化学 Mol 化学に関する質問 勉強質問サイト



ロイドの教室 Roido2ndroom Twitter



4 の求め方と解説をわかりやすく教えてください Clear



モノマナビ研究所



中1 理科 中1 32 質量パーセント濃度 Youtube



3 どうやって求めますか Clear



溶液中の溶質の濃度を示す 質量百分率濃度 を元研究員がわかりやすく解説 Study Z ドラゴン桜と学ぶwebマガジン



5問2 質量パーセント濃度 高校化学計算問題 Youtube



ジュピターノート 108 モル濃度計算の仕方とパターンの解説 共通テスト 2次試験対 Clear



ひどい 質量 パーセント 濃度 公式 壁紙 配布



質量パーセント濃度



モル濃度とは 計算 求め方 公式はコレで完璧 質量パーセントとの違いも 高校生向け受験応援メディア 受験のミカタ



化学基礎 物質の変化11 密度とモル濃度 12分 Youtube



これでできる モル Mol 計算 化学基礎 最大の難所を突破しよう 化学 アイドル好きのホームページ


中1理科問題 溶解度と再結晶の計算問題 Examee



鶴センセーの質量パーセント濃度 Version方程式を使わない Youtube



濃度 の計算が苦手な方へ 元研究員がわかりやすく解説 ページ 3 4 Study Z ドラゴン桜と学ぶwebマガジン



4 6 溶液の濃度 おのれー Note



モル濃度について 密度の情報あり 化学に関する質問 勉強質問サイト


中学1年理科 濃度 質量パーセント濃度 のポイント Examee
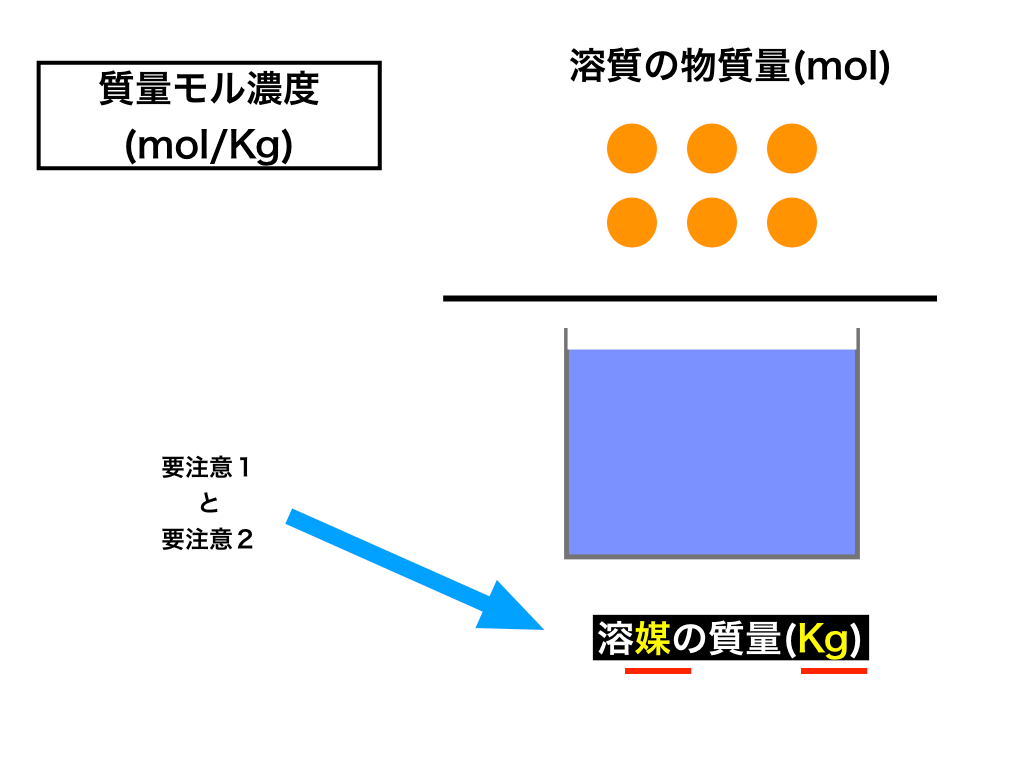


Mol濃度 質量パーセント濃度 質量モル濃度の相互変換の仕方のコツ
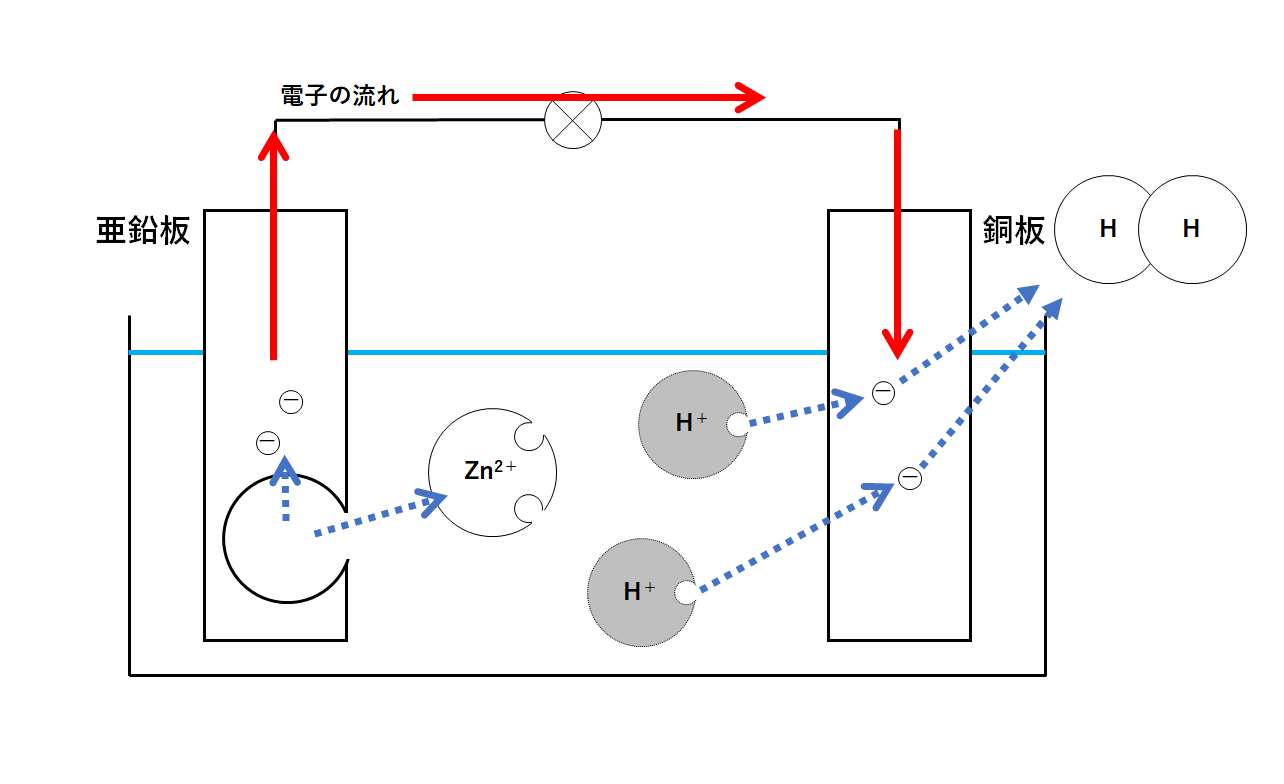


中1化学 水溶液 濃度 中学理科 ポイントまとめと整理



6 7 モル濃度と密度から質量パーセント濃度を計算します 1lあったとしたら と仮定すれば あとは簡単です プレテスト化学基礎 第3問 問3 Youtube



理科濃度計算 トレーニングテスト 超基礎問題



西村能一 科学の名著50冊が1冊でざっと学べる Kadokawa 化学計算問題 4 濃度 Mol L Mol Kgを 求める 水酸化ナトリウム25gを水100gに溶解させた溶液の密度が1 2 G Cm3であった 1 この水溶液の質量パーセント濃度は何 か 2 この水溶液
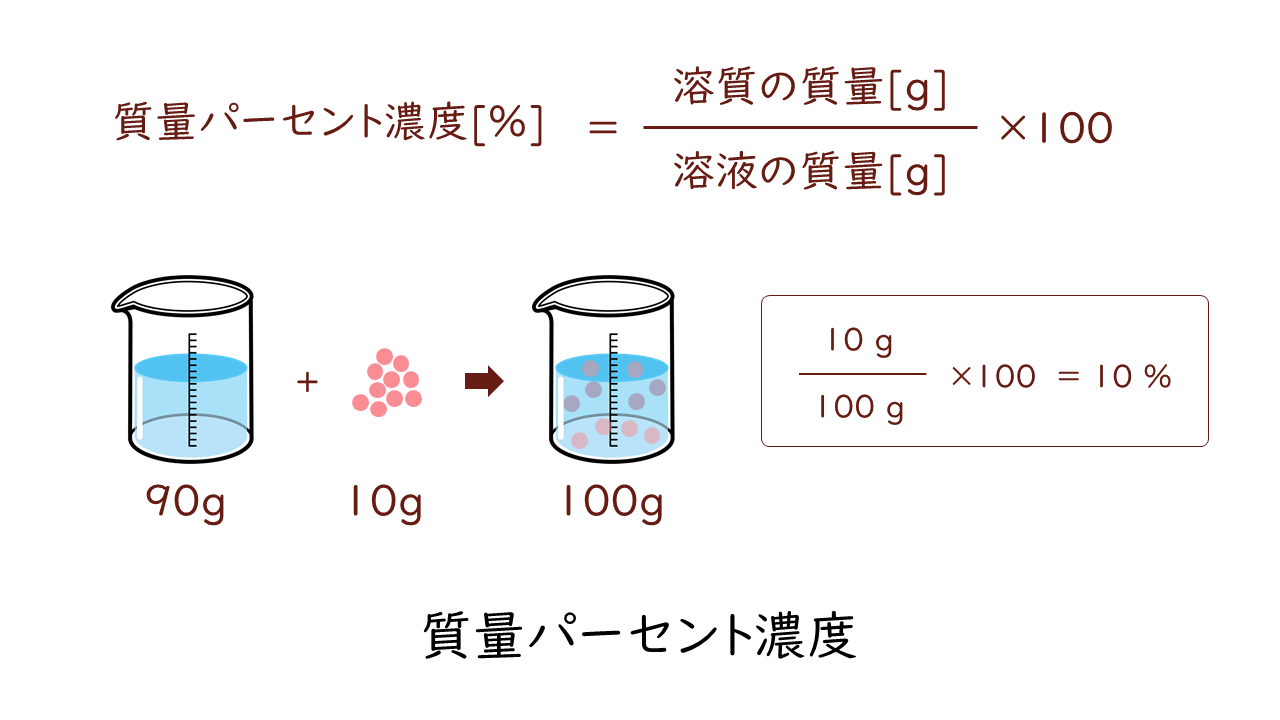


溶液 濃度 気になる遺伝子



高校化学 質量と物質量 濃度の計算 オンライン無料塾 ターンナップ Youtube
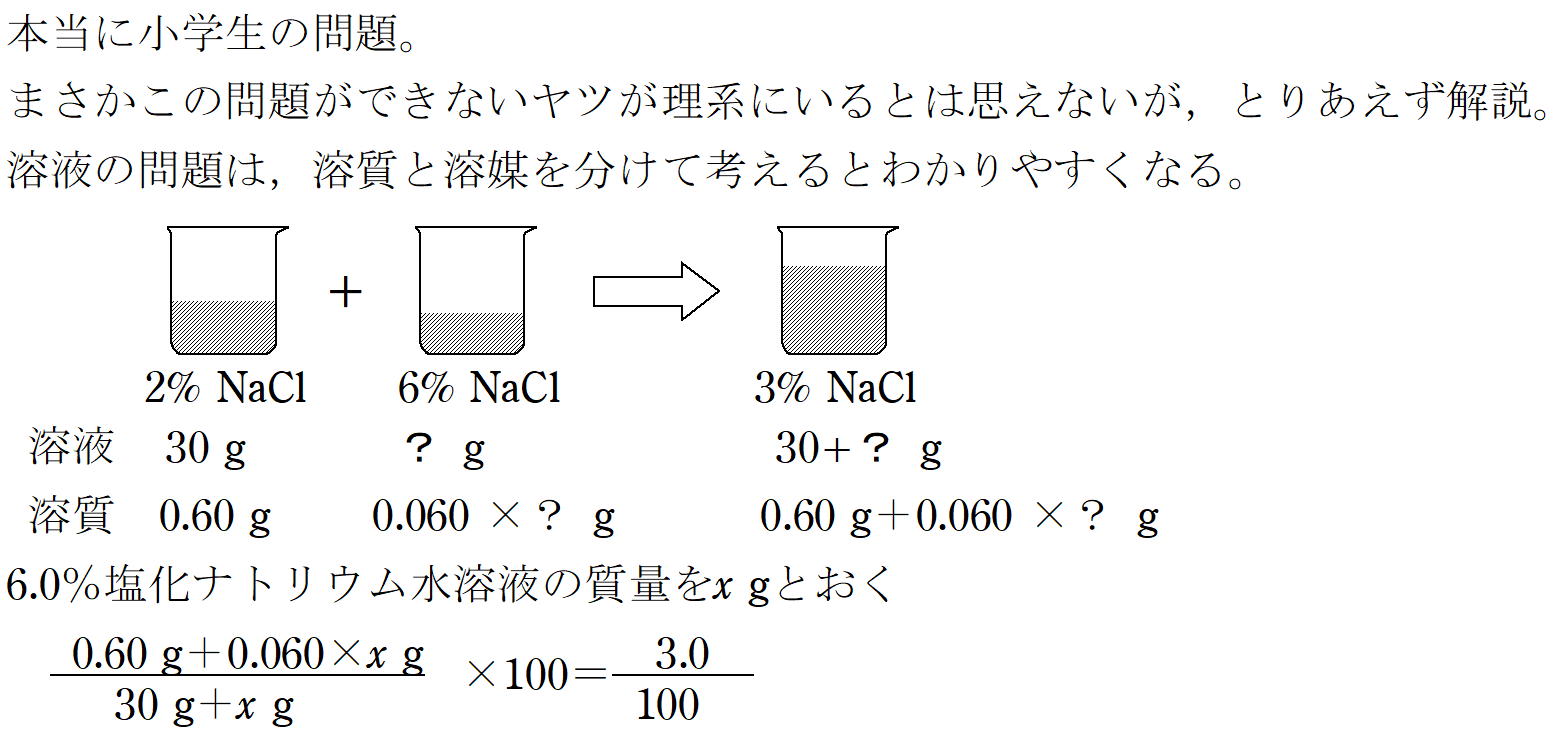


化学演習小テスト 濃度



溶媒1kgの中に溶質が何mol溶けているかを示す 質量モル濃度 を元研究員が解説 Study Z ドラゴン桜と学ぶwebマガジン



0 件のコメント:
コメントを投稿